Det tidlige 1900-tallet var en veldig lykkebringende tid for vitenskapene. I tillegg til at Ernest Rutherford og Niels Bohr fødte standardmodellen for partikkelfysikk, var det også en periode med gjennombrudd innen kvantemekanikk. Takket være pågående studier på elektroners oppførsel, begynte forskere å foreslå teorier der disse elementære partiklene oppførte seg på måter som trosset klassisk, Newtonsk fysikk.
Et slikt eksempel er Electron Cloud Model foreslått av Erwin Schrodinger. Takket være denne modellen ble ikke elektronene lenger avbildet som partikler som beveget seg rundt en sentral kjerne i en fast bane. I stedet foreslo Schrodinger en modell der forskere bare kunne komme med utdannede gjetninger om elektroners posisjon. Derfor kunne deres beliggenhet bare beskrives som en del av en 'sky' rundt kjernen der elektronene sannsynligvis blir funnet.
Atomfysikk til det 20. århundre:
De tidligste kjente eksemplene på atomteori kommer fra antikkens Hellas og India, der filosofer som Democritus postulerte at all materie var sammensatt av bittesmå, udelelige og uforgjengelige enheter. Begrepet “atom” ble myntet i antikkens Hellas og ga opphav til tankeskolen kjent som “atomisme”. Imidlertid var denne teorien mer et filosofisk begrep enn en vitenskapelig.
Det var først på 1800-tallet atomensteorien ble artikulert som en vitenskapelig sak, med de første evidensbaserte eksperimentene som ble utført. På begynnelsen av 1800-tallet brukte for eksempel den engelske forskeren John Dalton atombegrepet for å forklare hvorfor kjemiske elementer reagerte på visse observerbare og forutsigbare måter. Gjennom en serie eksperimenter med gasser, fortsatte Dalton med å utvikle det som er kjent som Daltons Atomic Theory.
Denne teorien utvidet lovene for samtale med masse og bestemte proporsjoner og kom ned til fem premisser: elementer, i deres reneste tilstand, består av partikler kalt atomer; atomene til et spesifikt element er alle de samme, helt til det siste atomet; atomer av forskjellige elementer kan fortelles fra hverandre med atomvektene; atomer av elementer forenes for å danne kjemiske forbindelser; atomer kan verken skapes eller ødelegges i kjemisk reaksjon, bare grupperinga endres noensinne.
Oppdagelse av elektron:
På slutten av 1800-tallet begynte forskere også å teoretisere at atomet var sammensatt av mer enn en grunnleggende enhet. Imidlertid våget de fleste forskere at denne enheten ville være på størrelse med det minste kjente atomet - hydrogen. På slutten av 1800-tallet ville hans endre seg drastisk, takket være forskning utført av forskere som Sir Joseph John Thomson.
Gjennom en serie eksperimenter med katodestrålerør (kjent som Crookes 'Tube), observerte Thomson at katodestrålene kunne avbøyes av elektriske og magnetiske felt. Han konkluderte med at de snarere enn å være sammensatt av lys, besto av negativt ladede partikler som var 1 ganger ganger mindre og 1800 ganger lettere enn hydrogen.

Dette motbeviste effektivt forestillingen om at hydrogenatom var den minste materieenheten, og Thompson gikk videre for å antyde at atomer var delbare. For å forklare at den totale ladningen til atomet, som besto av både positive og negative ladninger, foreslo Thompson en modell der de negativt ladede "kroppene" ble fordelt i et ensartet hav med positiv ladning - kjent som Plum Pudding Model.
Disse likene vil senere bli kalt "elektroner", basert på den teoretiske partikkelen som var forutsagt av den anglo-irske fysikeren George Johnstone Stoney i 1874. Og fra dette ble Plum Pudding Model født, så navngitt fordi den lignet den engelske ørkenen som består av plommekake og rosiner. Konseptet ble introdusert for verden i mars 1904-utgaven av Storbritannia Filosofisk magasin, til stor anerkjennelse.
Utvikling av standardmodellen:
Etterfølgende eksperimenter avslørte en rekke vitenskapelige problemer med Plum Pudding-modellen. For det første var det problemet med å demonstrere at atomet hadde en ensartet positiv bakgrunnsladning, som ble kjent som "Thomson-problemet". Fem år senere ble modellen motbevist av Hans Geiger og Ernest Marsden, som utførte en serie eksperimenter med alfapartikler og gullfolie - aka. "gullfolieeksperimentet."
I dette eksperimentet målte Geiger og Marsden spredningsmønsteret til alfapartiklene med en lysstoffrør. Hvis Thomsons modell var riktig, ville alfapartiklene passere gjennom atomstrukturen til folien uhindret. Imidlertid bemerket de i stedet at mens de fleste skjøt rett gjennom, var noen av dem spredt i forskjellige retninger, mens noen gikk tilbake i retning kilden.

Geiger og Marsden konkluderte med at partiklene hadde møtt en elektrostatisk kraft som var langt større enn den som tillates av Thomsons modell. Siden alfapartikler bare er heliumkjerner (som er positivt ladet), innebar dette at den positive ladningen i atomet ikke var vidt spredt, men konsentrert i et lite volum. I tillegg betydde det faktum at de partiklene som ikke ble avbøyet, passert gjennom uhindret at disse positive rommene ble adskilt av enorme tomter.
I 1911 tolket fysiker Ernest Rutherford Geiger-Marsden-eksperimentene og avviste Thomsons modell av atomet. I stedet foreslo han en modell der atomet besto av stort sett tomt rom, med all sin positive ladning konsentrert i sentrum i et veldig lite volum, som var omgitt av en sky av elektroner. Dette ble kjent som atomets Rutherford-modell.
Etterfølgende eksperimenter av Antonius Van den Broek og Niels Bohr foredlet modellen ytterligere. Mens Van den Broek antydet at atomnummeret til et element er veldig likt dets kjernefysiske ladning, foreslo sistnevnte en solsystem-lignende modell av atomet, der en kjerne inneholder atomnummeret av positiv ladning og er omgitt av en like antall elektroner i orbital-skjell (også kjent som Bohr-modellen).
Electron Cloud-modellen:
I løpet av 1920-årene ble den østerrikske fysikeren Erwin Schrodinger fascinert av teoriene Max Planck, Albert Einstein, Niels Bohr, Arnold Sommerfeld og andre fysikere. I løpet av denne tiden engasjerte han seg også innen feltene atomteori og spektre, og forsket ved Universitetet i Zürich og deretter Friedrich Wilhelm-universitetet i Berlin (hvor han etterfulgte Planck i 1927).

I 1926 taklet Schrödinger spørsmålet om bølgefunksjoner og elektroner i en serie papirer. I tillegg til å beskrive hva som ville bli kjent som Schrodinger-ligningen - en delvis differensialligning som beskriver hvordan kvantesystemets kvantetilstand endres med tiden - brukte han også matematiske ligninger for å beskrive sannsynligheten for å finne et elektron i en bestemt posisjon .
Dette ble grunnlaget for det som ville bli kjent som Electron Cloud (eller kvantemekanisk) modell, samt Schrodinger-ligningen. Basert på kvanteteori, som sier at all materie har egenskaper assosiert med en bølgefunksjon, skiller Electron Cloud Model seg fra Bohr-modellen ved at den ikke definerer den nøyaktige banen til et elektron.
I stedet forutsier det den sannsynlige plasseringen av elektronets plassering basert på en funksjon av sannsynligheter. Sannsynlighetsfunksjonen beskriver i utgangspunktet et skylignende område der elektronet sannsynligvis blir funnet, derav navnet. Der skyen er mest tett, er sannsynligheten for å finne elektronet størst; og hvor det er mindre sannsynlig at elektronet er, er skyen mindre tett.
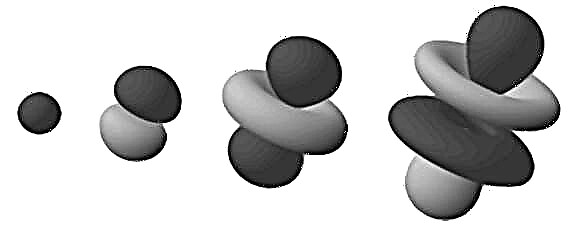
Disse tette regionene er kjent som "elektron-orbitaler", siden de er det mest sannsynlige stedet der et kretsende elektron vil bli funnet. Utvidet denne "sky" modellen til et tredimensjonalt rom, ser vi et vektstang eller blomsterformet atom (som på bildet øverst). Her er de forgrenende regionene de der vi mest sannsynlig finner elektronene.
Takket være Schrodingers arbeid, begynte forskere å forstå at det i kvantemekanikkens rike var umulig å vite nøyaktig posisjon og momentum for et elektron samtidig. Uansett hva observatøren først vet om en partikkel, kan de bare forutsi dens vellykkede beliggenhet eller fart når det gjelder sannsynligheter.
På ingen gitt tid vil de være i stand til å konstatere en av dem. Faktisk, jo mer de vet om momentumet til en partikkel, desto mindre vil de vite om dens beliggenhet, og omvendt. Dette er det som i dag er kjent som "Usikkerhetsprinsippet".
Legg merke til at orbitalene nevnt i forrige avsnitt er dannet av et hydrogenatom (dvs. med bare ett elektron). Når du arbeider med atomer som har flere elektroner, sprer elektronbaneområdene seg jevnt i en sfærisk uklar ball. Det er her begrepet ‘elektronsky’ er mest passende.
Dette bidraget ble universelt anerkjent som et av de viktige bidragene fra det 20. århundre, og som utløste en revolusjon innen fysikk, kvantemekanikk og faktisk alle vitenskaper. Fra nå av arbeidet forskere ikke lenger i et univers preget av absolutter av tid og rom, men i kvanteusikkerheter og tidsromsrelativitet!
Vi har skrevet mange interessante artikler om atomer og atommodeller her på Space Magazine. Her er hva er John Daltons atomodell ?, Hva er plommepuddingmodellen ?, Hva er Bohrs atommodell ?, Hvem var demokrat? Og hva er delene av et atom?
For mer informasjon, husk å sjekke Hva er kvantemekanikk? fra Live Science.
Astronomy Cast har også episode om temaet, som Episode 130: Radio Astronomy, Episode 138: Quantum Mechanics, og Episode 252: Heisenberg Uncerurity Principle